Come i batteri intestinali influenzano il trattamento del morbo di Parkinson
I pazienti con malattia di Parkinson sono trattati con levodopa, che viene convertita in dopamina, un neurotrasmettitore nel cervello. In uno studio pubblicato il 18 gennaio sulla rivista Nature Communications , gli scienziati dell'Università di Groningen mostrano che i batteri intestinali possono metabolizzare la levodopa in dopamina. Poiché la dopamina non può attraversare la barriera emato-encefalica, ciò rende il farmaco meno efficace, anche in presenza di inibitori che dovrebbero impedire la conversione della levodopa.
"È risaputo che i batteri intestinali possono influenzare il cervello", spiega l'Assistente Professor in Microbiologia Sahar El Aidy, capo ricercatore dello studio. "Esiste un dialogo chimico continuo tra i batteri intestinali e il cervello, il cosiddetto asse dell'intestino-cervello". La dottoressa El Aidy e il suo team hanno studiato la capacità del microbiota intestinale di influenzare la biodisponibilità della levodopa, un farmaco usato nel trattamento della malattia di Parkinson.
Barriera emato-encefalica
Il farmaco viene in genere assunto per via orale e la levodopa viene assorbita nell'intestino tenue e quindi trasportata attraverso il flusso sanguigno al cervello. Tuttavia, gli enzimi decarbossilasi possono convertire la levodopa in dopamina. A differenza della levodopa, la dopamina non può attraversare la barriera emato-encefalica, pertanto ai pazienti viene anche somministrato un inibitore della decarbossilasi. "Ma i livelli di levodopa che raggiungeranno il cervello variano notevolmente tra i pazienti affetti da malattia di Parkinson e ci siamo chiesti se il microbiota intestinale stesse giocando un ruolo in questa differenza", afferma El Aidy.
La biodisponibilità
Poiché ai pazienti con Parkinson viene somministrato un inibitore della decarbossilasi, il passo successivo è stato testare l'effetto di diversi inibitori della decarbossilasi umana sull'enzima batterico. "È emerso che, ad esempio, l'inibitore Carbidopa è oltre 10.000 volte più potente nell'inibire la decarbossilasi umana", afferma El Aidy.
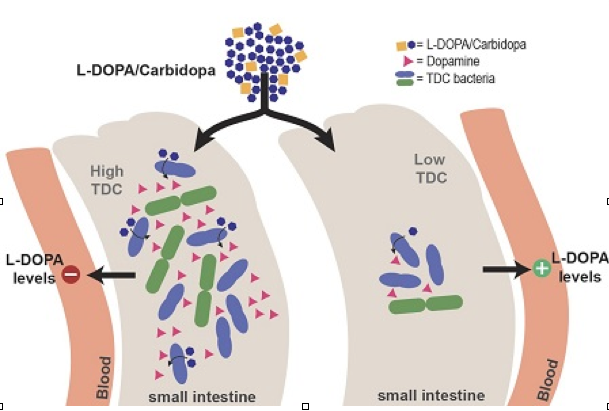
Questi risultati hanno portato il team all'ipotesi che la presenza di tirosina decarbossilasi batterica ridurrebbe la biodisponibilità della levodopa nei pazienti affetti da Parkinson. Per confermare questo, hanno testato campioni di feci da pazienti che avevano assunto una dose normale o elevata di levodopa. L'abbondanza relativa del gene batterico codificante per la tirosina decarbossilasi era correlata alla necessità di una dose più elevata del farmaco. "Poiché questi erano campioni di feci e la levodopa è assorbita nell'intestino tenue, questa non era ancora una prova solida. Tuttavia, abbiamo confermato la nostra osservazione dimostrando che la maggiore abbondanza di enzima batterico nel piccolo intestino dei ratti ha ridotto i livelli di levodopa nel sangue ", spiega El Aidy.
Circolo vizioso
Un altro risultato importante nello studio è la correlazione positiva tra durata della malattia e livelli di tirosina decarbossilasi batterica. Alcuni pazienti affetti da malattia di Parkinson sviluppano una crescita eccessiva di piccoli batteri intestinali, inclusi gli enterococchi, a causa del frequente assorbimento di inibitori della pompa protonica, che essi utilizzano per trattare i sintomi gastrointestinali associati alla malattia. Complessivamente, questi fattori determinano un circolo vizioso che porta ad un aumento del fabbisogno di dosaggio di inibitore della levodopa / decarbossilasi in un sottogruppo di pazienti.
El Aidy conclude che la presenza dell'enzima batterico tirosina decarbossilasi può spiegare perché alcuni pazienti hanno bisogno di dosaggi più frequenti di levodopa per trattare le loro fluttuazioni motorie. "Questo è considerato un problema per i malati di Parkinson, perché una dose più alta si tradurrà in discinesia, uno dei maggiori effetti collaterali del trattamento con levodopa."
Fonte: News Medical life sciences
https://www.rug.nl/sciencelinx/nieuws/2019/01/20190118_elaidy